服務(wù)熱線
18501696120
 更新時間:2025-10-30
更新時間:2025-10-30
 瀏覽次數(shù):33次
瀏覽次數(shù):33次
 更多推薦
更多推薦2025-10-31
2025-10-31
2025-10-31
2025-10-31
2025-10-30
2025-10-30
2025-10-30
2025-10-30
2025-08-27
2025-08-25

在藥物透皮吸收研究中,角質(zhì)層是繞不開的 "關(guān)卡"。它作為皮膚最外層的保護(hù)屏障,不僅決定了外界物質(zhì)能否進(jìn)入皮膚,還影響著藥物療效和護(hù)膚品功效的發(fā)揮。如何精準(zhǔn)測量活性成分在角質(zhì)層的深度分布、判斷其是否被去除,一直是科學(xué)家們的研究熱點(diǎn)。
德國薩爾大學(xué)Hahn T研究團(tuán)隊一項發(fā)表在《Skin Pharmacology and Physiology》的研究為這一難題提供了新方案 —— 紅外光密度測定法(IR-D),一種快速、非破壞性的檢測技術(shù),讓我們能更精準(zhǔn)地知道膠帶剝離后皮膚上殘留的角質(zhì)量。
皮膚是人體最大的器官,而角質(zhì)層(stratum corneum,SC)是皮膚的 "第一道防線"。它由多層死亡的角質(zhì)細(xì)胞組成,像一道致密的 "城墻",既能防止水分流失,又能阻擋外界有害物質(zhì)入侵。
對于藥物研發(fā)來說,很多外用藥需要穿過角質(zhì)層才能發(fā)揮作用;對于護(hù)膚品而言,有效成分能否滲透到目標(biāo)層次(比如美白成分到達(dá)基底層、保濕成分停留在角質(zhì)層)直接決定了產(chǎn)品效果;而在毒理學(xué)評估中,還要評估有害物質(zhì)是否會通過角質(zhì)層進(jìn)入體內(nèi)。
因此,搞清楚有效成分在角質(zhì)層中的深度分布,以及如何確定角質(zhì)層是否被去除(避免過度剝離損傷皮膚或剝離不足導(dǎo)致數(shù)據(jù)不準(zhǔn)),是透皮相關(guān)實驗研究的難題之一。
目前,研究角質(zhì)層常用的方法是 "膠帶剝離法":用粘性膠帶反復(fù)粘貼皮膚,每層膠帶會粘下部分角質(zhì)層,通過分析每層膠帶上的角質(zhì)量,就能推斷活性物質(zhì)在角質(zhì)層的深度分布。
但這個方法有兩個難點(diǎn)需要解決:
1. 如何準(zhǔn)確測量每層膠帶上的角質(zhì)量?
2. 如何判斷什么時候皮膚角質(zhì)層被剝離(該停手了)?
傳統(tǒng)方法存在不少問題:
• 重量法:通過稱重膠帶前后的重量差計算角質(zhì)層量,但容易受汗液、皮膚油脂、制劑殘留影響,誤差大;
• 染色法:用染料(如臺盼藍(lán))染色后測吸收,但靈敏度低,且膠帶本身可能著色,干擾結(jié)果;
• 蛋白質(zhì)測定法(如 BCA 法):這是目前的 "金標(biāo)準(zhǔn)",通過檢測角質(zhì)層中的蛋白質(zhì)含量推算其量,但需要把膠帶放入化學(xué)試劑中提取蛋白質(zhì),屬于破壞性檢測 —— 測完后膠帶就不能再用于分析藥物或護(hù)膚品成分了,還耗時(至少幾個小時)。
這些問題讓角質(zhì)層研究效率低、成本高,也影響了數(shù)據(jù)的準(zhǔn)確性。
科學(xué)家們找到了一種更高效的方法 —— 紅外光密度測定法(IR-D),儀器工具是Labodorf 850C皮膚角質(zhì)量測試儀。

(Labodorf 850C皮膚角質(zhì)量測試儀)
它的測量原理是:用 850nm 的紅外光照射粘有角質(zhì)層的膠帶,測量光穿過膠帶后的吸光強(qiáng)度變化(稱為 "偽吸收",類似光被角質(zhì)層散射、反射導(dǎo)致的強(qiáng)度下降)。研究發(fā)現(xiàn),這種 "偽吸收" 的強(qiáng)度和角質(zhì)層中的蛋白含量成線性關(guān)系 —— 也就是說,通過光強(qiáng)度變化,就能快速算出膠帶上的角質(zhì)層量。
和傳統(tǒng)方法相比,它的優(yōu)勢一目了然:
• 非破壞性:膠帶不用被化學(xué)試劑處理,測完后還能用于分析藥物或護(hù)膚品成分含量;
• 快速:貼完膠帶穩(wěn)定3分鐘左右,放入儀器瞬間出結(jié)果,無需等待幾小時;
• 精準(zhǔn):不受皮膚油脂、汗液影響,也不用考慮染色干擾。
為了驗證紅外法角質(zhì)量測試的可靠性,研究團(tuán)隊做了一系列實驗,從體內(nèi)到體外,測試比對。
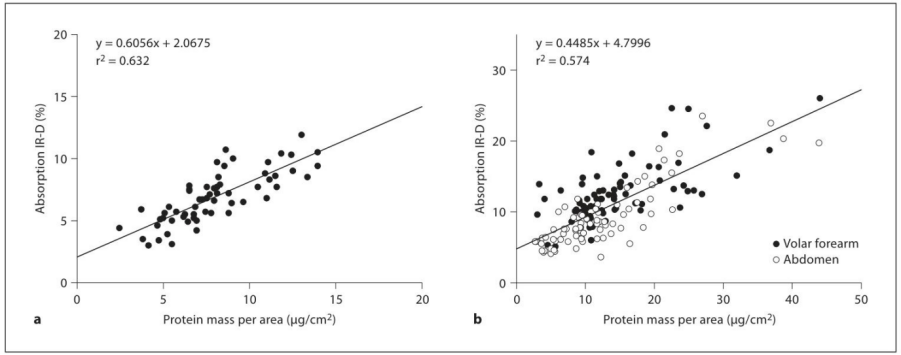
研究先在志愿者身上做了實驗:用兩種常見膠帶(Tesa 透明膠帶和D-Squame 膠帶),分別在小臂內(nèi)側(cè)和腹部進(jìn)行剝離,然后用 IR-D 和 BCA 法(金標(biāo)準(zhǔn))對比。
結(jié)果顯示:兩種方法的結(jié)果高度吻合(相關(guān)系數(shù) r2 最高達(dá) 0.63),而且不管是哪種膠帶、哪個部位(小臂、腹部),IR-D 都能穩(wěn)定工作。這說明它在人體皮膚上的測量是靠譜的。
研究的重點(diǎn)是體外實驗(皮膚來自經(jīng)過德國萊巴赫市慈善醫(yī)院倫理委員會批準(zhǔn)的整形手術(shù)的人體皮膚樣本),團(tuán)隊測試了兩種皮膚:
• 新鮮的離體皮膚;
• 冷凍儲存 1 周、1 個月、3 個月的皮膚(模擬實驗室常見的樣本儲存情況)。
實驗證明:無論是新鮮皮膚還是冷凍 3 個月的皮膚,850C皮膚角質(zhì)量測試儀測量得到的角質(zhì)層深度和 BCA 法幾乎一致。這意味著,即使皮膚樣本被冷凍保存,依然有效測試,解決了實驗室樣本儲存后的檢測難題。
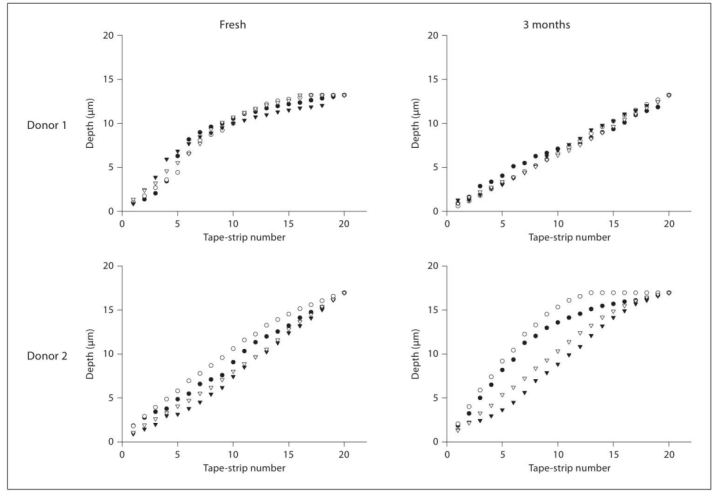
兩位不同捐贈者的腹部皮膚經(jīng)連續(xù)膠帶剝離后到達(dá)的角質(zhì)層(SC)深度。使用tesa膠帶在體外對新鮮未冷凍的皮膚以及在-26°C下儲存3個月的皮膚進(jìn)行了膠帶剝離實驗。空心符號代表通過紅外密度測定法(IR-D)計算得出的深度,實心符號代表通過BCA測定法計算得出的深度。每個時間點(diǎn)、每位捐贈者均取2個皮膚活檢樣本,每個樣本進(jìn)行20次連續(xù)膠帶剝離。圓圈=皮膚活檢樣本A;三角形=皮膚活檢樣本B。
在過去實驗研究人員一般憑經(jīng)驗決定剝離多少次膠帶(通常 20-100次),但每個人的角質(zhì)層厚度不同,同一人的不同部位也有差異,固定次數(shù)很容易導(dǎo)致 "過度剝離"(損傷皮膚)或 "剝離不足"(角質(zhì)層沒去干凈),最終導(dǎo)致實驗數(shù)據(jù)離散、重現(xiàn)性差。
IR-D 的一個大亮點(diǎn)是:它能通過 "定量下限(LLOQ)" 判斷角質(zhì)層是否去除。實驗發(fā)現(xiàn),當(dāng) IR-D 的信號低于 LLOQ 時,剩余的角質(zhì)層不到總量的 5%,可以認(rèn)為已經(jīng)剝離。
這意味著,以后不用再靠 "猜" 來決定貼多少層膠帶了 —— 儀器會實時告訴你:"好了,可以停了"
綜合所有實驗,IR-D法 展現(xiàn)出三個特點(diǎn):
1. 非破壞性:同一膠帶既能用 IR-D 測角質(zhì)層深度,又能后續(xù)分析藥物或護(hù)膚品成分濃度,方便快捷;
2. 實時監(jiān)測:在實驗中根據(jù)皮膚樣本情況隨時調(diào)整剝離次數(shù),避免主觀判斷;
3. 適用范圍廣:不管是新鮮皮膚還是冷凍儲存的皮膚,不管是哪種膠帶、哪個身體部位,都能測量。
對于透皮給藥研發(fā)而言,能加速透皮藥物的研發(fā)過程,明確藥物有效成分在角質(zhì)層的分布規(guī)律;對于護(hù)膚品研發(fā)來說,它能更精準(zhǔn)地測試成分在皮膚中的滲透深度,指導(dǎo)產(chǎn)品配方優(yōu)化;對于毒理學(xué)研究,能更高效地評估有害物質(zhì)的皮膚滲透風(fēng)險。
角質(zhì)層雖薄,卻是皮膚研究的 "重中之重"。紅外光密度測定法的出現(xiàn),解決了傳統(tǒng)方法耗時、破壞性強(qiáng)、準(zhǔn)確性不足的問題,為透皮吸收研究提供了全新的工具。
未來,隨著技術(shù)的普及,我們或許能看到更多基于精準(zhǔn)皮膚滲透數(shù)據(jù)的藥品和護(hù)膚品 —— 畢竟,只有真正 "看穿" 角質(zhì)層的秘密,才能讓有效成分更精準(zhǔn)地發(fā)揮作用。
參考文獻(xiàn):
1. Kalia YN, Pirot F, Guy RH: Homogeneous transport in a heterogeneous membrane: water diffusion across human stratum corneum in vivo. Biophys J 1996; 71: 2692–2700.
2. Russell LM, Wiedersberg S, Bego?a Delgado-Charro M: The determination of stratumcorneum thickness. An alternative approach. Eur J Pharm Biopharm 2008; 69: 861–870.
3. Netzlaff F, Kostka KH, Lehr CM, Schaefer UF: TEWL measurements as a routine method for evaluating the integrity of epidermis sheets in static Franz type diffusion cells in vitro. Limitations shown by transport data testing. Eur J Pharm Biopharm 2006; 63: 44–50.
4.Hahn T, Hansen S, Neumann D, Kostka KH, Lehr CM, Muys L, Schaefer UF. Infrared densitometry: a fast and non-destructive method for exact stratum corneum depth calculation for in vitro tape-stripping. Skin Pharmacol Physiol. 2010;23(4):183-92.
 返回列表
返回列表